正确率60.0%svg异常
B
A.$${{N}{{a}_{2}}{{O}_{2}}}$$中$${{O}}$$元素的化合价为$${{−}{2}}$$价
B.由$${{N}{a}}$$生成$${{N}{{a}_{2}}{{O}_{2}}}$$的反应是氧化还原反应
C.$${{a}}$$溶液与过量$${{C}{{O}_{2}}}$$气体反应生成$${{N}{{a}_{2}}{C}{{O}_{3}}}$$
D.$${{N}{{a}_{2}}{C}{{O}_{3}}}$$的电离方程式:$$\mathrm{N a_{2} C O_{3}==N a_{2}^{+}+C O_{3}^{2-}}$$
2、['化合价', '电离方程式', '表示粒子构成的符号的含义及相关计算', '原(离)子结构示意图']正确率60.0%下列化学用语正确的是()
A
A.中子数为$${{1}{8}}$$的氯原子:$$\mathrm{^{3 5}_{1 7} C l}$$
B.$${{N}{{H}_{4}}{C}{l}}$$中$${{N}}$$的化合价为$${{+}{3}}$$价
C.svg异常
D.$$\mathrm{N a H C O_{3}}$$的电离方程式:$$\mathrm{N a H C O_{3}}=\mathrm{=N a^{+}+H^{+}+C O_{3}^{2-}}$$
3、['化合价', '氧化还原反应的几组概念', '硫及其化合物的相互转化']正确率60.0%svg异常
C
A.硫元素在自然界中既有游离态又有化合态
B.过程⑤可在土壤的缺氧区实现
C.循环过程中硫元素只被还原
D.若生物体有机硫中硫元素为$${{−}{2}}$$价,则过程③中$$\mathrm{S O_{4}^{2-}}$$发生的是还原反应
4、['化合价', '元素金属性和非金属性强弱的比较方法', '同一主族内元素性质递变规律与原子结构的关系']正确率60.0%下列说法中,不符合第Ⅶ$${{A}}$$族元素性质的特征的是()
A
A.从上到下,元素的非金属性逐渐增强
B.易形成$${{−}{1}}$$价阴离子
C.除$${{F}}$$外,最高价氧化物对应的水化物显酸性
D.从上到下,气态氢化物的稳定性依次减弱
5、['化合价', '晶体熔、沸点高低的比较规律', '元素金属性和非金属性强弱的比较方法', '微粒半径大小的比较', '元素的推断及综合应用']正确率40.0%$${{W}}$$、$${{X}}$$、$${{Y}}$$、$${{Z}}$$四种元素组成的化合物是新能源汽车电池的正极材料,$${{W}}$$、$${{X}}$$、$${{Y}}$$、$${{Z}}$$的原子序数依次增大,$${{W}}$$和$${{Z}}$$是两种金属元素,$${{Z}}$$单质是用途最广泛的金属,$${{X}}$$、$${{Y}}$$形成的$$\mathrm{Y X}_{4}^{3-}$$有$${{5}{0}}$$个电子。下列说法正确的是()
C
A.$${{W}}$$的简单离子半径大于$${{H}^{−}}$$的半径
B.在同周期元素的氢化物中,$${{X}}$$的氢化物沸点最高
C.$${{Y}}$$的最高价氧化物对应的水化物的酸性强于碳酸
D.$${{Z}}$$元素在化合物中只有$${{+}{2}}$$、$${{+}{3}}$$价
6、['化合价', '元素金属性和非金属性强弱的比较方法', '氢键的存在对物质性质的影响']正确率40.0%类推的思维方法在化学学习与研究中经常用到,但有时会产生错误的结论。因此,推出的结论最终要经过实践的检验才能决定其是否正确。以下几种类推结论中,正确的是()
B
A.$${{I}{V}{A}}$$族元素氢化物沸点顺序是:$$\mathrm{G e H_{4}} > \mathrm{S i H_{4}} > \mathrm{C H_{4}}$$;则$${{V}{A}}$$族元素氢化物沸点顺序也是:$$\mathrm{A s H_{3} > P H_{3} > N H_{3}}$$
B.第二周期元素氢化物的稳定性顺序是:$$\mathrm{H F} > \mathrm{H_{2} O} > \mathrm{N H_{3}} ;$$则第三周期元素氢化物的稳定性顺序也是: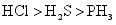
C.$${{F}{e}_{3}{{O}_{4}}}$$可以写成$$\mathrm{F e O} \cdot\mathrm{F e_{2} O_{3}}$$;$${{P}{b}_{3}{{O}_{4}}}$$也可以写成$$\mathrm{P b O} \cdot\mathrm{P b}_{2} \mathrm{O_{3}}$$
D.$$\mathrm{N a H S O_{4}}$$与$$\mathrm{N a H S O_{3}}$$溶于水显酸性,则所有酸式盐溶于水显酸性
7、['化合价', '离子方程式的书写', '氮及其化合物的转化关系', '氮的固定']正确率40.0%svg异常
D
A.svg异常
B.svg异常
C.转化过程中$${{N}{O}^{−}_{3}}$$被甲醇氧化为$${{N}_{2}}$$
D.svg异常
8、['化工工艺流程实验', '化合价', '二氧化硫的性质', '氨水的组成及性质', '大气污染的治理原理及方法', '亚硫酸及亚硫酸盐']正确率40.0%svg异常
B
A.$${{X}}$$可能含有$${{2}}$$种盐
B.$${{a}}$$是$${{S}{{O}_{3}}}$$
C.$${{Y}}$$可能含有$$\mathrm{( N H_{4} )}_{2} \mathrm{S O}_{4}$$
D.$$\mathrm{( N H_{4} )}_{2} \mathrm{S}_{2} \mathrm{O}_{8}$$中$${{S}}$$的化合价不可能为$${{+}{7}}$$
9、['化合价', '结构式', '元素金属性和非金属性强弱的比较方法', '微粒半径大小的比较', '元素的推断及综合应用']正确率60.0%svg异常
D
A.简单离子半径:$$\mathbf{Z} > \mathbf{Y} > \mathbf{X}$$
B.最简单氢化物稳定性:$$\mathbf{Z} > \mathbf{Y} > \mathbf{X}$$
C.含氧酸酸性:$${{Z}{>}{Y}}$$
D.$${{Y}{X}{{Z}_{2}}}$$中$${{Y}}$$的化合价为$${{+}{4}}$$
10、['化合价']正确率80.0%“酒驾”是当前热门话题之一.交巡警检查驾驶员是否饮酒的仪器里装有$$\mathrm{K_{2} C r_{2} O_{7}}$$,$$\mathrm{K_{2} C r_{2} O_{7}}$$中$${{C}{r}}$$元素的化合价为$${{(}{)}}$$
C
A.$${{+}{2}}$$价
B.$${{+}{5}}$$价
C.$${{+}{6}}$$价
D.$${{+}{7}}$$价
1. 解析:
A选项错误,$$Na_2O_2$$中O元素的化合价为$$-1$$价(过氧根离子$$O_2^{2-}$$)。
B选项正确,Na与$$O_2$$反应生成$$Na_2O_2$$时,Na的化合价升高,属于氧化还原反应。
C选项错误,$$Na_2O_2$$与过量$$CO_2$$反应生成$$Na_2CO_3$$和$$O_2$$,而非$$Na_2CO_3$$。
D选项错误,$$Na_2CO_3$$的电离方程式应为$$Na_2CO_3 = 2Na^+ + CO_3^{2-}$$。
2. 解析:
A选项正确,中子数为18的氯原子表示为$$^{35}_{17}Cl$$(质量数=质子数+中子数)。
B选项错误,$$NH_4Cl$$中N的化合价为$$-3$$价。
D选项错误,$$NaHCO_3$$的电离方程式应为$$NaHCO_3 = Na^+ + HCO_3^-$$,$$HCO_3^-$$进一步电离为$$H^+ + CO_3^{2-}$$。
3. 解析:
A选项正确,硫在自然界中以单质(如火山口)和化合物(如硫酸盐)形式存在。
B选项正确,过程⑤(硫酸盐还原为$$H_2S$$)可在缺氧土壤中由微生物完成。
C选项错误,硫循环中既有还原(如$$SO_4^{2-} \to H_2S$$)也有氧化(如$$H_2S \to S$$)过程。
D选项正确,若有机硫中S为$$-2$$价,$$SO_4^{2-}$$转化为$$-2$$价需被还原。
4. 解析:
A选项错误,第ⅦA族从上到下非金属性逐渐减弱(F > Cl > Br > I)。
B选项正确,卤素易得电子形成$$-1$$价阴离子。
C选项正确,除F外,Cl、Br、I的最高价含氧酸(如$$HClO_4$$)为酸性。
D选项正确,气态氢化物稳定性随非金属性减弱而降低(HF最稳定)。
5. 解析:
根据题意,Z为Fe(用途最广的金属),$$YX_4^{3-}$$有50个电子,推测Y为P(磷酸根$$PO_4^{3-}$$),X为O。W为Li或Na(正极材料常用元素)。
A选项错误,$$Li^+$$或$$Na^+$$半径均小于$$H^-$$。
B选项错误,$$H_2O$$的沸点高于同周期氢化物(如$$HF$$),但题目中X为O,$$H_2O$$确实沸点最高。
C选项正确,$$H_3PO_4$$酸性强于$$H_2CO_3$$。
D选项错误,Fe在化合物中还有其他价态(如$$+6$$价高铁酸盐)。
6. 解析:
A选项错误,$$NH_3$$因氢键沸点反常高于$$PH_3$$。
B选项正确,第三周期氢化物稳定性:$$HCl > H_2S > PH_3$$,与非金属性一致。
C选项错误,$$Pb_3O_4$$实际为$$2PbO \cdot PbO_2$$,Pb显$$+2$$和$$+4$$价。
D选项错误,$$NaHCO_3$$等酸式盐溶于水显碱性。
7. 解析:
C选项正确,硝酸根($$NO_3^-$$)被甲醇还原为$$N_2$$(N从$$+5$$价降至0价)。
8. 解析:
D选项正确,S最高价为$$+6$$,$$(NH_4)_2S_2O_8$$中S为$$+6$$价(过氧键$$-O-O-$$的O为$$-1$$价)。
9. 解析:
B选项正确,非金属性越强,氢化物越稳定(如O > N > C)。
C选项错误,含氧酸酸性需具体分析(如$$HNO_3$$强于$$H_2CO_3$$,但$$H_2SO_3$$不一定强于$$HNO_2$$)。
10. 解析:
C选项正确,$$K_2Cr_2O_7$$中Cr为$$+6$$价($$2 \times (+1) + 2x + 7 \times (-2) = 0$$,解得$$x = +6$$)。
.jpg)